Physique-Chimie Cycle 4
Nouveau manuel de Sciences et Technologie 6e
Découvrez cet ouvrage collaboratif, conforme au nouveau programme !
Mes Pages
Thème 1 - Organisation et transformations de la matière
Ch. 1
L'eau que nous buvons est-elle pure ?
Ch. 2
La matière : états, masse et volume
Ch. 3
Les changements d'état de la matière
Ch. 4
Les mélanges
Ch. 5
La matière à l'échelle microscopique
Ch. 6
Que trouve-t-on dans l'air ?
Ch. 7
Les transformations chimiques et la pollution
Ch. 8
Modélisation des transformations chimiques
Ch. 9
Les ions dans notre quotidien
Ch. 10
Quand les acides et les bases réagissent
Ch. 11
Introduction à la masse volumique
Ch. 12
La masse volumique
Ch. 13
La matière, dans l'espace et dans l'Univers
Ch. 14
De l'Univers aux atomes
Thème 2 - Mouvement et interactions
Ch. 15
Introduction à la vitesse et au mouvement
Ch. 16
Repérage de mouvement et mesure de vitesse
Ch. 17
Vitesse et mouvement
Ch. 18
Les interactions
Ch. 19
Les forces
Ch. 20
Le poids
Thème 3 - L'énergie et ses conversions
Ch. 21
Introduire la notion d'énergie
Ch. 22
Conversion et transfert de l'énergie
Ch. 23
La conservation de l'énergie
Ch. 24
Les circuits électriques
Ch. 25
La tension et l'intensité
Ch. 26
Relations entre grandeurs dans les circuits électriques
Ch. 27
Résistance et loi d'Ohm
Ch. 28
Puissance et énergie en électricité
Thème 4 - Des signaux pour observer et communiquer
Ch. 29
Le son
Ch. 30
La lumière
Ch. 31
Vitesse de propagation des signaux
Ch. 32
Des signaux au-delà de la perception humaine
Chapitre 2
Bilan
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Compétence : Travailler en autonomie.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
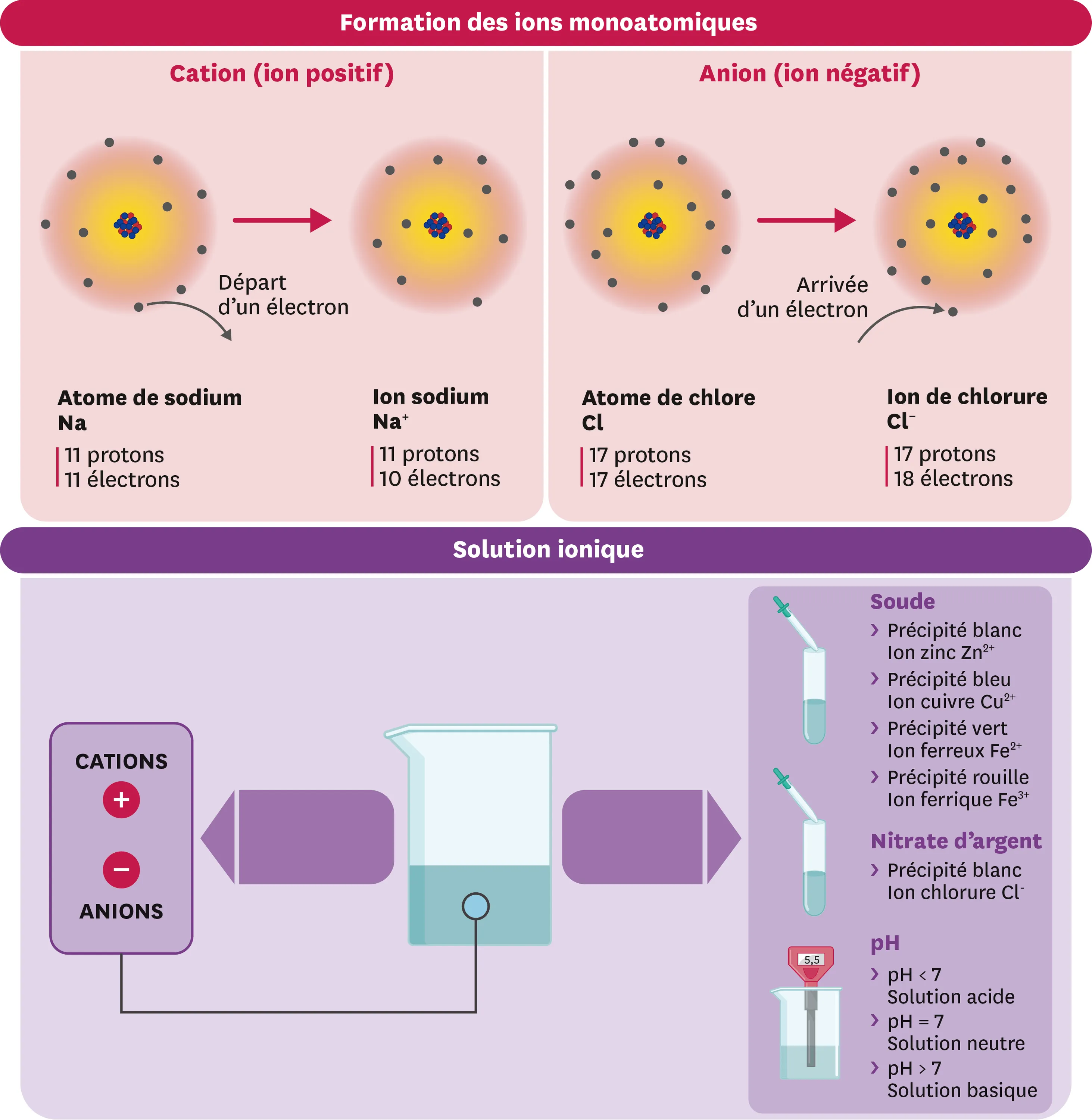
1Nature des ions
- Un ion est un atome ou une molécule qui a perdu ou gagné un ou plusieurs électrons.
- Le gain d'un ou plusieurs électrons donne un ion négatif : un anion. Par exemple, l'atome de chlore Cl gagne un électron pour devenir l'ion chlorure Cl−.
- La perte d'un ou plusieurs électrons donne un ion positif : un cation. Par exemple, l'atome de cuivre Cu perd deux électrons pour devenir l'ion cuivre Cu2+.
Le saviez-vous ?
Les ions sont les espèces chimiques obtenues après le gain ou la perte d'au moins un électron par une molécule ou un atome.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
2Détection des ions
- La présence d'ions peut être établie à l'aide de tests par précipitation. Un précipité apparait lorsque le test est positif ; la couleur du précipité permet d'identifier l'ion concerné.
- Les solutions d'hydroxyde de sodium (soude) permettent de tester la présence de plusieurs ions monoatomiques métalliques.
- Les solutions de nitrate d'argent permettent de tester la présence des ions chlorure.
Le saviez-vous ?
Une des méthodes d'identification d'un ion dans une solution consiste à former un précipité en ajoutant un réactif test : un autre ion en solution.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
3Solides et solutions ioniques
- Un solide ionique est un assemblage régulier d'anions et de cations.
- Une solution ionique est une solution de cations et d'anions, le plus souvent aqueuse. Sa formule s'écrit entre parenthèses avec les formules des ions qu'elle contient. Ex. : (Fe3+ + 3 Cl-).
- Les proportions en anions et en cations rendent les solides et solutions ioniques électriquement neutres.
Le saviez-vous ?
La proportion d'anions et de cations dans un composé ionique dépend de leur charge électrique respective. Le solide formé ou la solution obtenue sont nécessairement neutres.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
4pH et ions
- Le pH varie entre 0 et 14, et se mesure avec un pH-mètre ou du papier pH.
- Le pH vaut lorsqu'il y a autant d'ions hydrogène H+ que d'ions hydroxyde HO-. La solution est alors neutre d'un point de vue acido-basique.
- Plus le pH est inférieur à 7, plus la solution est acide et contient d'ions hydrogène H+.
- Plus le pH est supérieur à 7, plus la solution est basique et contient d'ions hydroxyde HO-.
Le saviez-vous ?
Le pH d'une solution indique si celle-ci est acide, basique ou neutre. Cela dépend des proportions d'ions hydrogène et hydroxyde.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
- Un anion : activité 3.
- Un cation : activité 3.
- Un précipité : activité 2.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Je retiens par l'image

Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille
