Chapitre 1
Activité 2 - en groupe
Vie terrestre et évolution de l'atmosphère
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Introduction
Les plus anciennes traces d'êtres vivants sur Terre sont datées de 3,5 milliards d'années (Ga). Elles correspondent à des traces d'organismes unicellulaires marins.
Quelles caractéristiques de l'atmosphère ont permis l'apparition de la vie ?
Quelles sont les interactions entre les êtres vivants et l'atmosphère ?
Quelles sont les interactions entre les êtres vivants et l'atmosphère ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Document commun à tous les groupes
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
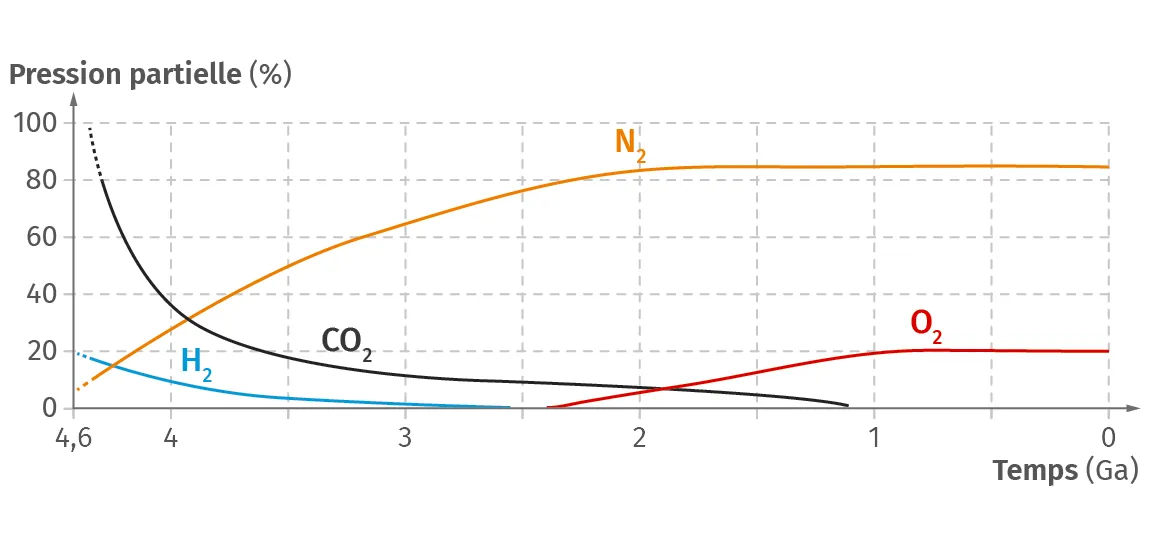
Doc. 1Évolution de la pression partielle de différents gaz au cours du temps

Supplément numérique
Retrouvez plus d'informations sur l'évolution naturelle du
.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Groupe 1 Les formations de fers rubanés
Physique-chimie
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 2Formation de fers rubanés


Exploitées comme gisement de fer, les formations de fer rubané (BIF pour banded iron formations) résultent de l'oxydation du fer présent dans les océans, entre -3,8 Ga à -2,0 Ga.
Quand la plus grande partie du fer a été oxydée en ions fer (III) \text{Fe}^{3+}, la teneur en dioxygène a augmenté dans les océans.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Oxydation de l'élément fer
Matériel nécessaire :
béchers,
sulfate de fer (\text{FeSO}_4) solide ou solution de sulfate de fer (II) (\text{Fe}^{2+}(aq) ; \text{SO}_4^{2-}(aq)),
solution d'hydroxyde de sodium (\text{Na}^+(aq) ; \text{HO}^-(aq)) à 0{,}1 mol⋅L-1,
bulleur à dioxygène,
spatule.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 3Oxydation du fer
Le dioxygène est un oxydant fort, c'est-à-dire qu'il peut réagir avec de nombreuses espèces chimiques dites réductrices selon une réaction d'oxydoréduction. C'est notamment le cas du fer. Celui-ci réagit avec le dioxygène pour former des oxydes de fer (de formule générale \text{Fe}_x \text{O}_y et pouvant être rouges). On dénombre trois oxydes de fer différents : \text{FeO}, \text{Fe}_2\text{O}_3 et \text{Fe}_3\text{O}_4. Les équations modélisant ces transformations sont :
4\ \text{Fe} + 3\ \text{O}_2 \to 2\ \text{Fe}_2\text{O}_3
2\ \text{Fe} + \text{O}_2 \to 2\ \text{FeO}
3\ \text{Fe} + 2\ \text{O}_2 \to \text{Fe}_3\text{O}_4
2\ \text{Fe} + \text{O}_2 \to 2\ \text{FeO}
3\ \text{Fe} + 2\ \text{O}_2 \to \text{Fe}_3\text{O}_4
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Indicateur de réussite
Avoir mis en relation l'origine de la formation des BIF et l'augmentation du dioxygène dans l'atmosphère.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Groupe 2 Stromatolites et production de dioxygène
SVT
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 4Les stromatolites : des structures mixtes
Les stromatolites sont des structures à la fois géologiques (roches carbonatées) et biologiques (formes proches des cyanobactéries) que l'on trouve dans les mers chaudes et peu profondes. Ils présentent un métabolisme photosynthétique et produisent donc du dioxygène. Des formes actuelles existent, mais on retrouve aussi des fossiles datant de 3,5 Ga, ce qui en fait les plus anciennes formes de vie connues.


Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 5Organisation des stromatolites

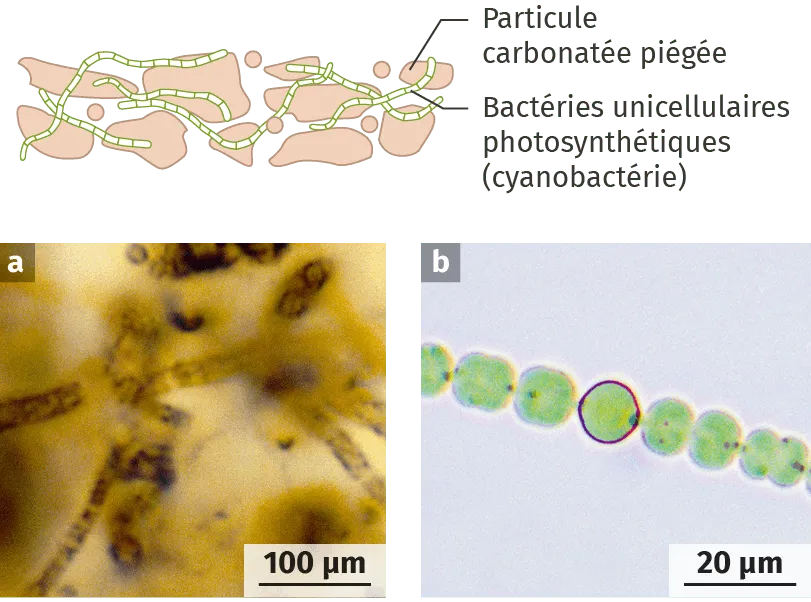
Supplément numérique
Partez à la découverte des stromatolites en Argentine :
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Indicateur de réussite
Avoir fait le lien entre l'apparition de la vie et la formation du dioxygène dans l'atmosphère.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Groupe 3 Un aperçu du cycle de l'oxygène
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Doc. 6Respiration et photosynthèse participent aux transferts de dioxygène


Les végétaux réalisent respiration et photosynthèse.

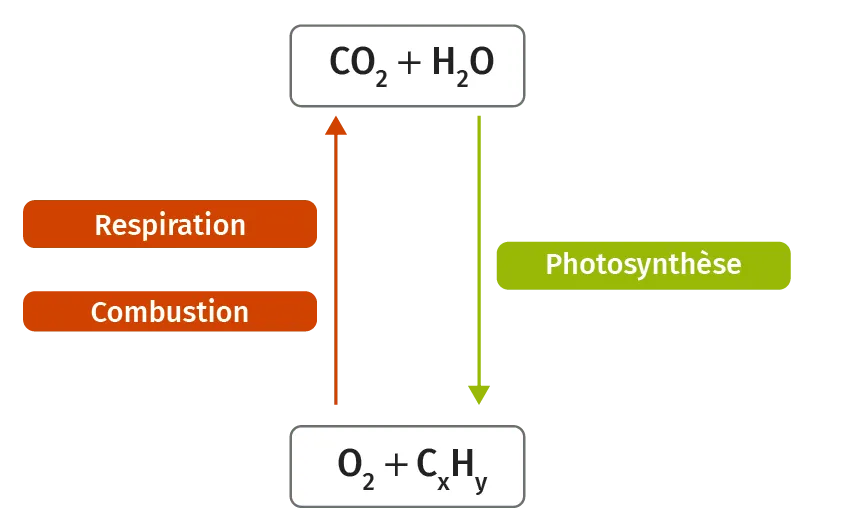
Les phénomènes de respiration, de photosynthèse et de combustion consomment et libèrent du dioxygène et du dioxyde de carbone. Les éléments qui consomment du dioxygène sont des puits, ceux qui en libèrent sont des sources.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Plus d'informations sur ces phénomènes :
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Indicateur de réussite
Avoir identifié les principaux puits et sources de dioxygène.
Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille

