Physique-Chimie 1re Spécialité
Rejoignez la communauté !
Co-construisez les ressources dont vous avez besoin et partagez votre expertise pédagogique.
Mes Pages
1. Constitution et transformations de la matière
Ch. 1
Composition chimique d'un système
Ch. 2
Composition chimique des solutions
Ch. 3
Évolution d'un système chimique
Ch. 4
Réactions d'oxydoréduction
Ch. 5
Détermination d'une quantité de matière par titrage
Livret Bac : Thème 1
Ch. 6
De la structure à la polarité d'une entité
Ch. 7
Interpréter les propriétés d’une espèce chimique
Ch. 8
Structure des entités organiques
Ch. 9
Synthèse d'espèces chimiques organiques
Ch. 10
Conversions d'énergie au cours d'une combustion
Livret Bac : Thème 1 bis
2. Mouvement et interactions
Ch. 11
Modélisation d'interactions fondamentales
Ch. 12
Description d'un fluide au repos
Ch. 13
Mouvement d'un système
Livret Bac : Thème 2
3. L'énergie, conversions et transferts
Ch. 14
Études énergétiques en électricité
Ch. 15
Études énergétiques en mécanique
Livret Bac : Thème 3
4. Ondes et signaux
Ch. 16
Ondes mécaniques
Ch. 17
Images et couleurs
Ch. 18
Modèles ondulatoire et particulaire de la lumière
Livret Bac : Thème 4
Méthode
Fiches méthode
Fiche méthode compétences
Annexes
Chapitre 6
De la structure à la polarité d'une entité
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Problématique


Linus Pauling, prix Nobel de chimie en 1954.
Quelle est la contribution remarquable de ce scientifique dans notre connaissance de la liaison chimique ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
À revoir pour bien commencer
- ❯ Configuration électronique et électrons de valence
- ❯ Stabilité des gaz nobles, ions monoatomiques
- ❯ Modèle de la liaison covalente, lecture de schémas de Lewis de molécules
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
Objectifs du chapitre
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.
1. La règle de l'octet :
2. La formule de Lewis d'une molécule :
3. Tous les éléments d'une même ligne de la classification périodique appartiennent à la même et tous les éléments d'une même colonne appartiennent à la même .
4. La formule de Lewis de l'éthanol \text{CH}_3-\text{CH}_2-\text{OH} est :
2. La formule de Lewis d'une molécule :
3. Tous les éléments d'une même ligne de la classification périodique appartiennent à la même
4. La formule de Lewis de l'éthanol \text{CH}_3-\text{CH}_2-\text{OH} est :
5. Après avoir établi les configurations électroniques des différents éléments ci-dessous, associer chaque élément à sa description, sans consulter le tableau périodique des éléments.
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.

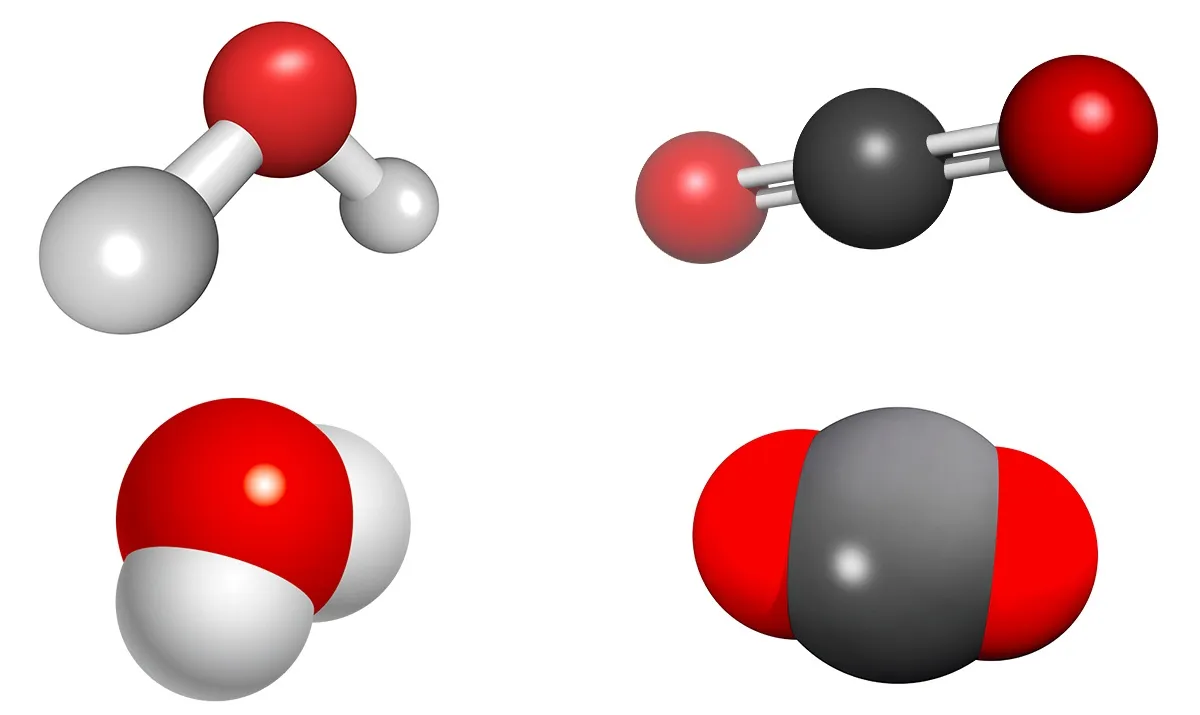
La molécule d'eau et la molécule de dioxyde de carbone sont toutes les deux constituées de trois atomes. Elles possèdent pourtant des géométries dans l'espace très différentes.
Comment peut-on expliquer cette différence ?
Comment peut-on expliquer cette différence ?
Ressource affichée de l'autre côté.
Faites défiler pour voir la suite.
Faites défiler pour voir la suite.


Une erreur sur la page ? Une idée à proposer ?
Nos manuels sont collaboratifs, n'hésitez pas à nous en faire part.
j'ai une idée !
Oups, une coquille
